
原子の構造

今回から早速、危険物取扱者乙4類の化学基礎の勉強を始めていきましょう。

早速ですが、まずは基礎の中の基礎である『原子と周期表』について学んでいきましょう

よろしくお願いしまっ!

姉さんは、こんな感じのイラストを見た事がありますか?
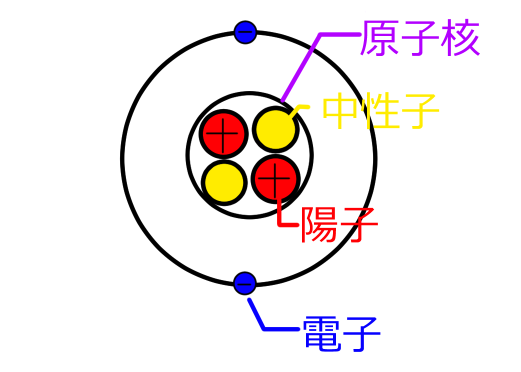

もちろんだよ!原子の構造を表したイラストだよね!

真ん中に、『陽子』と『中性子』からできてる『原子核』ってのがあるんだよね!

んで、その原子核の周りを『電子』が回ってるんだよね!

その通りです。素晴らしいです。

それでは電荷というものがあったのを覚えていますか?

あー、デンカね。デンカデンカ。
炊飯器とかケトルとかだよね。

それは電化製品の電化ですね。

電荷とは電気的な偏りのこと
要は、陽子はプラスの電気を帯びていて、電子はマイナスの電気を帯びているという事です。


あー、なんかあった気がする。

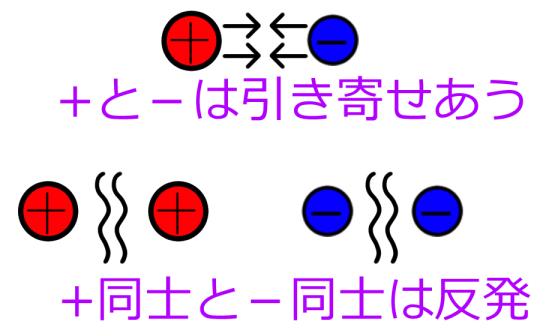
重要なのは、プラスとマイナスで引き寄せ合い、プラス同士、マイナス同士で反発するという点です

電子がどっかへ飛んでいかず、ずっと原子の周りを回ってるのは、
陽子と電子で引き寄せあってるからなわけですね。

それから、原子は基本的に陽子と電子をセットで持っています。

なので、後述のイオンのような例外を除いて、陽子と電子の数はイコールになります
周期表ってなんだ?

さて、次は原子とは切っても切れない関係にある周期表について見ていきましょう。


うわぁぁぁぁああああ!!目がぁぁああああ!!

急にどうしたんですか?頭大丈夫ですか?

せめて頭じゃなくて目を心配してくれよ

私、法則性のある表を見ると、アレルギーで拒絶反応が出るんだよ

局所的なアレルギーですね。

この周期表というのは、簡単に言うと『原子を原子番号順に並べた表』です。

はぇー。原子って一杯種類があるんだね!

さて、姉さん。気になりませんか?気になりますよね?

うん?何が?

この真ん中の空白の部分です。なんというか、もっと、こう、綺麗に並べて欲しくありませんか?


妹ちゃん、A型出てんなー!

ボクは宇宙人なので、血液型とかないですし、あれは迷信だと思っています。

そもそも原子番号とは、何を基準に決められているか、ご存知ですか?

適当なんじゃね。世の中そんなもんでしょ

そんなわけないです。
原子番号は、陽子と電子の数で決まります。

たしか陽子と電子の数は一緒になるんだよね。じゃあ、1個ずつの場合は原子番号は1になるって事?

その通りです。
周期表の見方

次は簡単に周期表の見方を確認していきましょうか。

例えば、原子番号10番のネオンです。Neが元素記号で、その隣に2つの数字が書かれています


下の10は原子番号だとして、その上にある20ってのはなんだ?

これは質量数といって、簡単に言うと原子の重さを表します。

いずれ詳しく触れますので、今は気にしなくていいですよ。

ほーん。じゃあさ、この元素記号って言うのは、どうやって決まってるの?

大体はラテン語かギリシア語の頭文字を取っています。

たとえば、ネオンであれば、ギリシア語で『新しい』を意味する『neos』から取ったとされています
なんで周期表って名前なの?

ところで姉さん。気になりませんか?気になりますよね?

気になるって、一体何がだね?

なぜ、周期表という名前なのでしょうか。

原子を番号順に並べたものなら、原子表とか原子番号表とかの方がわかりやすいと思いませんか?

たしかに。適当な名前を付けるなんて、地球人は愚かだね

いえ、ちゃんと理由があります。

実は、原子番号順で並べた際、一定周期で似た性質の原子が現れるという特性があるのです。

そうなんだ。具体的には、どんなものがあるの?

例えば、原子番号2番のヘリウム、原子番号10番のネオン、原子番号18番のアルゴン

これらの原子は『希ガス』と呼ばれ、非常に安定していて、化学反応を起こしにくい気体である、という性質を持っています。
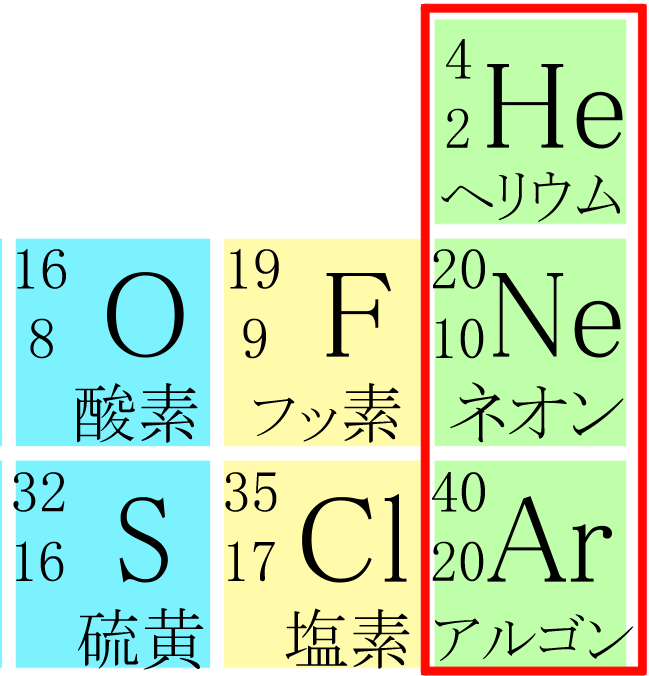
↑アルゴンの原子番号20になってるけど正しくは18だよ!べ、別に直すのめんどうとか、そんな事ないんだからね!
by犬星さん(中の人)

へえ、8番ごとにに似た性質の原子が出てきてるんだね。

しかも、この3つの原子は、同じ縦の列に並んでいるね!

このように、周期表の縦列には、似た性質の原子が並ぶようになっているのです。

同じ性質の現れる周期ごとに、並べたものだから、周期表っていう名前なんだね、
電子の層

さて姉さん…気になりますよね?

気になりますよね構文だね。今度は何が気になるって言うのさ?

なぜ、周期的に似た性質の原子が現れるのか。気になりますよね?

ちゃんと理由があるんだね

それを理解するためには、電子について、より深く理解する必要があります。

先程名前の出た原子番号10番のネオンを例に考えてみましょう。


姉さん、試しにネオンの原子構造をいてみてください。

ネオンは原子番号10番なので、電子と陽子が10個ずつあります。また、中性子の数も10個とします

任せてよ!

まず、原子核の中に陽子と中性子を10個書きます!

次にその周りに電子を10個書きます

できた!ネオンの原子構造!
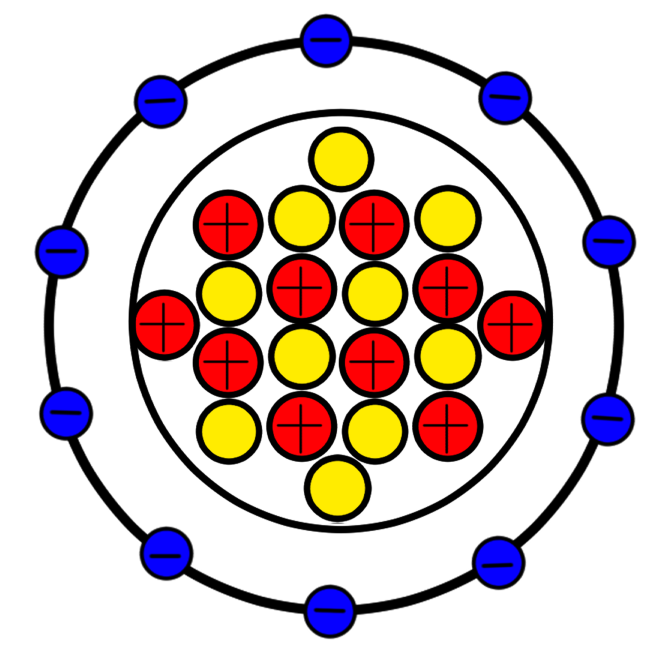

残念。不正解です。

正しいネオンの原子構造はこのようになります。
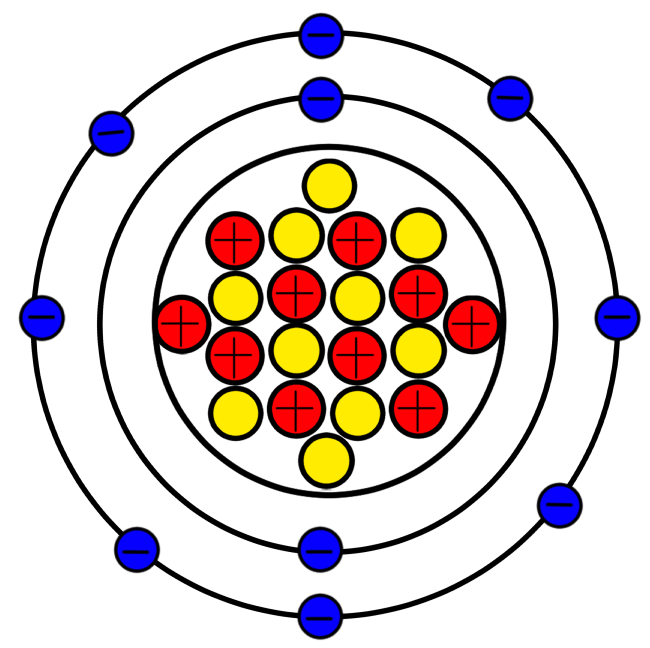

電子が二重になってるんだけどー!騙したなー!

別に騙してはいないです。

このように電子は複数の層に成します。これは1周あたり存在できる原子の数に限りがあるためです。

じゃあ、1層目には、電子が2つしか入らないから、残りの8個は2層目になってるってこと?

その通りです。

1周目は2個まで。
2週目と3週目は8個までしか、電子は入る事ができないのです。
周期表の縦列と横列

そういえば、先程の原子達の原子番号は、ヘリウムが2番、ネオンが10番、アルゴンが18番でしたね?

加えて、原子番号、電子の数、陽子の数は等しくなるんでしたね。

あ、私気付いちゃったよ!

それぞれ、1層目、2層目、3層目に満杯まで電子が詰まってるよ!

1層目なら2個まで、2層目は8個までだから、合わせて10個まで!
んで、3層目も8個まで入るから、合計で18個まで電子が入るよ!
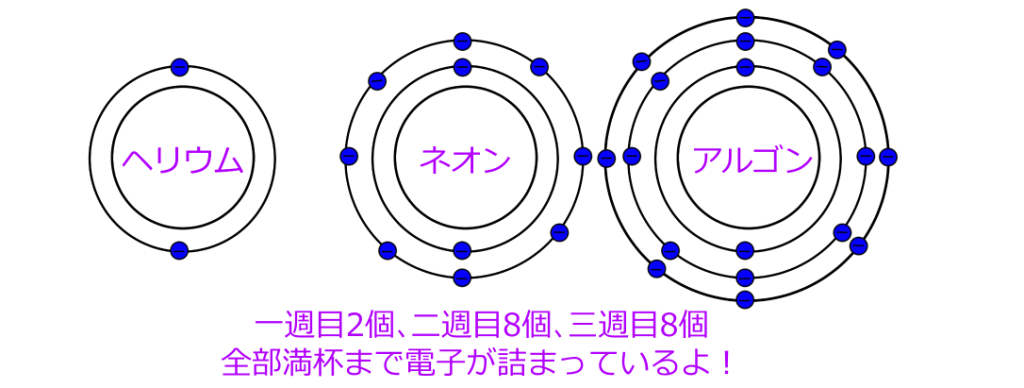

そうですね。2個、10個、18個と、原子番号と一致しますね。

では、一旦ここで周期表を確認してみましょう。

ヘリウムは横1行目、ネオンは横2行目、アルゴンは横3行目のそれぞれ右端にあるのがわかりますね?
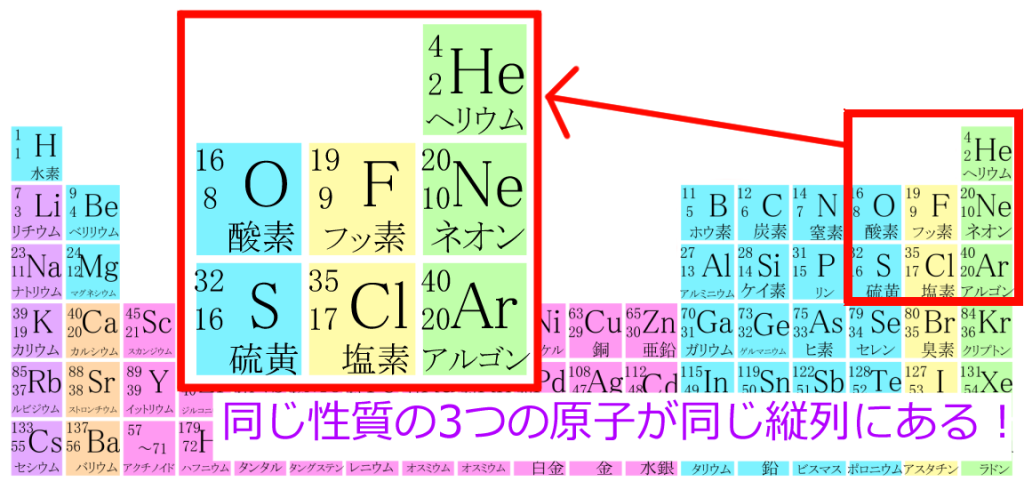
↑アルゴンの原子番号が20番になってるけど、正しくは18番だよ!by犬星さん

つまりこの横の行は、電子の層がいくつあるかを表してるのかな?
ヘリウムが一周、ネオンは二周、アルゴンは三周あるよ!

そうですね。加えて、それぞれが左から何番目にあるかを数えてみてください。

ヘリウムが2番目、ネオンが8個、アルゴンが8個だね!

つまり縦列は一番外側の層に電子がいくつあるかを表しているって事だね!

その通りです。

周期表からは、その原子の持つ電子の配置についても読み取ることができるのです。

例えば、原子番号20番のカルシウムは、横4列目の左から2番目にあります。

すると、電子の配列が下記のようになる事がわかります。

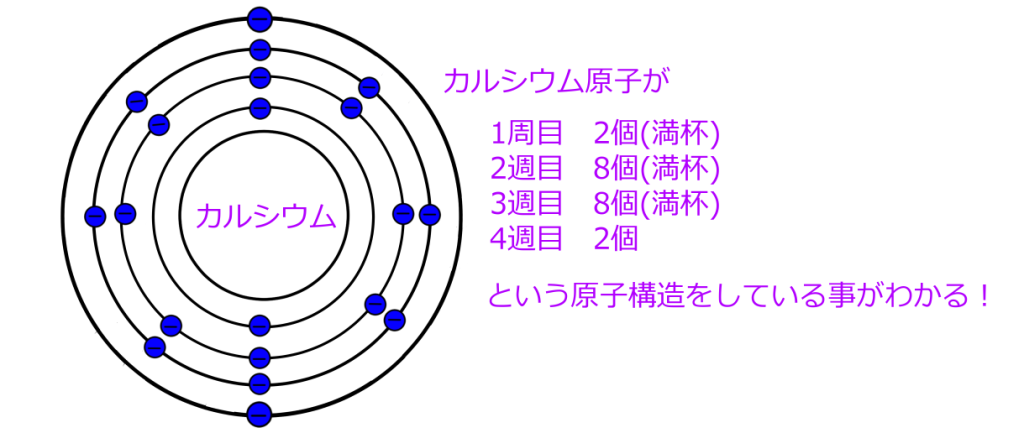

3列目の18個までは満杯に詰まっていて、残り2個は4層目にあるね!

周期表って、ただのよく分からん表だと思ってたけど、実は凄い便利なものなんだね!

さて、そうなると周期表に空白がある理由もわかりますね?

周期表の横列が電子の層に対応してて、層ごとに入れる電子の数が違うからだよね!

1周目は2個しか入らないけど、2層目は8個まで入るから、6個空白ができちゃうんだね!

その通りです。電子の性質上、空白ができるのは仕方ないわけです。
まとめ

さて、周期表について段々詳しくなってきましたね。

さて、最後の疑問である『周期的に同じ性質の原子が現れる理由」について説明していきたいのですが…

ですが…?

少し長くなってしまいそうなので、今回はこれで終わりにします。

最後に本日のまとめを載せておきますね。




コメント